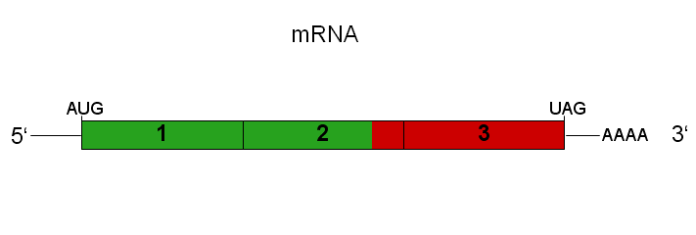
На відміну від звичайної мРНК вакцини яка кодує лише цільові антигени, самоампліфікуючі мРНК (saRNA) також кодують неструктурні білки та промотор, що робить saRNAs реплікони, здатні до транскрипції in vivo в клітинах господаря. Перші результати вказують на те, що їхня ефективність, коли вони вводяться в менших дозах, є на рівні з ефективністю звичайних доз традиційних мРНК. Завдяки низьким вимогам до дози, меншій кількості побічних ефектів і більшій тривалості дії saRNA виглядає як краща РНК-платформа для вакцин (зокрема для версії 2.0 мРНК COVID-вакцин) і новіших терапевтичних засобів. Жодна вакцина або препарат на основі саРНК ще не схвалені для використання людиною. Однак значний прогрес у цій галузі може стати початком ренесансу в профілактиці та лікуванні інфекцій і дегенеративних розладів.
Зайве говорити, що людство слабке перед такими пандеміями, як COVID. Ми всі це пережили і так чи інакше вплинули на нас; мільйони не могли дожити до наступного ранку. Враховуючи, що в Китаї також була масштабна програма імунізації проти COVID-19, останні повідомлення ЗМІ про стрибки випадків захворювання та смертності в Пекіні та навколо нього викликають занепокоєння. Необхідність готовності та невпинного прагнення до більш ефективного вакцини і терапевтику неможливо недооцінити.
Надзвичайна ситуація, створена пандемією COVID-19, дала можливість для перспективного РНК технологія вийти з віку. Клінічні випробування можуть бути завершені рекордними темпами мРНК на основі COVID Вакцини, BNT162b2 (виробництва Pfizer/BioNTech) і мРНК-1273 (від Moderna) отримав EUA від регуляторів і згодом відіграв важливу роль у забезпеченні захисту від пандемії людей, особливо в Європі та Північній Америці1. Ці мРНК вакцини засновані на синтетичних РНК платформах. Це забезпечує швидке, масштабоване промислове виробництво без клітин. Але це не без обмежень, таких як висока вартість, холодний ланцюг постачання, зниження титру антитіл тощо.
мРНК вакцини зараз використовується (іноді його називають звичайним або 1-го покоління мРНК вакцини) засновані на кодуванні вірусного антигену в синтетичній РНК. Невірусна система доставки транспортує транскрипт до цитоплазми клітини-господаря, де експресується вірусний антиген. Потім експресований антиген індукує імунну відповідь і забезпечує активний імунітет. Оскільки РНК легко розкладається і ця мРНК у вакцині не може самотранскрибуватись, для виклику бажаної імунної відповіді у вакцину необхідно ввести значну кількість транскриптів синтетичної вірусної РНК (мРНК). Але що, якщо транскрипт синтетичної РНК включає також неструктурні білки та промоторні гени на додаток до бажаного вірусного антигену? Такий РНК транскрипт матиме здатність до транскрипції або самопосилення під час транспортування в клітину-хазяїна, хоча він буде довшим і важчим, а його транспорт до клітин-господарів може бути більш складним.
На відміну від звичайних (або не підсилювальних) мРНК який має коди лише для цільового вірусного антигену, самопідсилювального мРНК (saRNA), має здатність транскрибувати себе in vivo в клітинах господаря завдяки наявності необхідних кодів для неструктурних білків і промотора. МРНК-вакцини-кандидати на основі мРНК, що самоампліфікуються, називають другим або наступним поколінням мРНК вакцини. Вони пропонують кращі можливості з точки зору вимог до менших доз, відносно меншої кількості побічних ефектів і більшої тривалості дії/ефектів (2-5). Обидві версії РНК-платформи відомі науковому співтовариству вже деякий час. У відповідь на пандемію дослідники обрали нереплікаційну версію платформи мРНК для розробки вакцини з огляду на її простоту та гостроту пандемічної ситуації, а також щоб набути досвіду з неампліфікуючою версією, оскільки це виправдано з обережності. Зараз ми маємо дві затверджені мРНК вакцини проти COVID-19, а також кілька вакцин і терапевтичних препаратів, які плануються, наприклад Вакцина проти ВІЛ та лікування Хвороба Шарко-Марі-Тута.
кандидати на вакцину saRNA проти COVID-19
Інтерес до вакцини saRNA не новий. За кілька місяців після початку пандемії, в середині 2020 року, Маккей та ін. представив вакцину-кандидата на основі saRNA, яка показала високі титри антитіл у мишачих сироватках і хорошу нейтралізацію вірусу6. Клінічне випробування фази 1 VLPCOV–01 (самопосилювальний РНК кандидат на вакцину) на 92 здорових дорослих, результати яких були опубліковані на препринті минулого місяця, дійшли висновку, що введення низьких доз цього saRNA вакцина-кандидат індукує імунну відповідь, порівнянну зі звичайною мРНК-вакциною BNT162b2, і рекомендує її подальший розвиток як бустерну вакцину7. В іншому нещодавно опублікованому дослідженні, проведеному в рамках клінічного випробування COVAC1 для розробки стратегії введення бустерної дози, було виявлено кращу імунну відповідь у людей, які раніше хворіли на COVID-19 і отримали нову самопідсилювальну РНК (saRNA) Вакцина проти COVID-19 плюс вакцина, дозволена Великобританією8. Доклінічні випробування нової пероральної вакцини-кандидата на основі самопідсилення РНК на моделі миші викликав високий титр антитіл9.
saRNA кандидат на вакцину проти грипу
Грип вакцини наразі використовуються на основі інактивованих вірусів або синтетичних рекомбінантних (синтетичний ген HA у поєднанні з бакуловірусом)10. Самопідсилювальний мРНКВакцина-кандидат може індукувати імунітет проти кількох вірусних антигенів. Доклінічні випробування біцистронної вакцини sa-mRNA A/H5N1 проти грипу на мишах і тхорах викликали потужні антитіла та відповідь Т-клітин, що вимагало оцінки на людях у клінічних випробуваннях11.
Вакцини проти COVID-19 привернули увагу зі зрозумілих причин. Деякі доклінічні роботи щодо застосування платформ РНК були проведені для інших інфекцій та неінфекційних розладів, таких як рак, хвороба Альцгеймера та спадкові розлади; однак жодна вакцина або препарат на основі саРНК ще не схвалені для використання людиною. Необхідно провести більше досліджень щодо використання вакцин на основі saRNA, щоб всебічно зрозуміти їх безпеку та ефективність для використання на людях.
***
Список використаної літератури:
- Прасад У., 2020. МРНК-вакцина проти COVID-19: віха в науці та кардинальна зміна в медицині. Науковий європейський. Опубліковано 29 грудня 2020 р. Доступно онлайн за адресою http://scientificeuropean.co.uk/medicine/covid-19-mrna-vaccine-a-milestone-in-science-and-a-game-changer-in-medicine/
- Bloom, K., van den Berg, F. & Arbuthnot, P. Самоампліфікуючі РНК-вакцини для інфекційних захворювань. Джин Тер 28, 117–129 (2021). https://doi.org/10.1038/s41434-020-00204-y
- Пурсейф М.М та ін 2022. Самоампліфікуючі мРНК-вакцини: механізм дії, дизайн, розробка та оптимізація. Відкриття наркотиків сьогодні. Том 27, Випуск 11, листопад 2022 р., 103341. DOI: https://doi.org/10.1016/j.drudis.2022.103341
- Блекні А.К та ін 2021. Оновлення щодо розробки вакцини мРНК із самоампліфікацією. Вакцини 2021, 9(2), 97; https://doi.org/10.3390/vaccines9020097
- Анна Блекні; Наступне покоління РНК-вакцин: самоампліфікуюча РНК. Biochem (Лондон) 13 серпня 2021 р.; 43 (4): 14–17. зробити: https://doi.org/10.1042/bio_2021_142
- Маккей П.Ф., Ху К., Блекні А.К. та ін. Кандидат у вакцину на основі ліпідних наночастинок РНК із самоампліфікацією SARS-CoV-2 індукує високі титри нейтралізуючих антитіл у мишей. Nat Commun 11, 3523 (2020). https://doi.org/10.1038/s41467-020-17409-9
- Акахата В. та ін. 2022. Безпека та імуногенність вакцини SARS-CoV-2, що самоампліфікується РНК, що експресує закріплений RBD: рандомізоване, сліпе дослідження фази 1. Препринт medRxiv 2022.11.21.22281000; Опубліковано 22 листопада 2022 р. doi: https://doi.org/10.1101/2022.11.21.22281000
- Елліот Т та ін. (2022) Посилення імунної відповіді після гетерологічної вакцинації вакцинами проти COVID-19 РНК та мРНК, що самоампліфікуються. Патог PLoS 18(10): e1010885. Опубліковано: 4 жовтня 2022 р. DOI: https://doi.org/10.1371/journal.ppat.1010885
- Кейха, Р., Хашемі-Шахрі, С. М. та Джебалі, А. Оцінка нових пероральних вакцин на основі наночасток ліпідів РНК, що самоампліфікуються (saRNA LNP), LNP Lactobacillus plantarum, трансфікованих saRNA, і Lactobacillus plantarum, трансфікованих saRNA, для нейтралізації SARS-CoV -2 варіанти альфа і дельта. Sci Rep 11, 21308 (2021). Опубліковано: 29 жовтня 2021 р. https://doi.org/10.1038/s41598-021-00830-5
- CDC 2022. Як виготовляються вакцини проти грипу. Доступно онлайн за адресою https://www.cdc.gov/flu/prevent/how-fluvaccine-made.htm доступні на 18 грудня 2022.
- Chang C. та ін., 2022. Біцистронні вакцини проти грипу мРНК, що самоампліфікуються, підвищують перехресно-реактивні імунні відповіді у мишей і запобігають інфекції у тхорів. Методи молекулярної терапії та клінічні розробки. Том 27, 8 грудня 2022 р., сторінки 195-205. https://doi.org/10.1016/j.omtm.2022.09.013
***