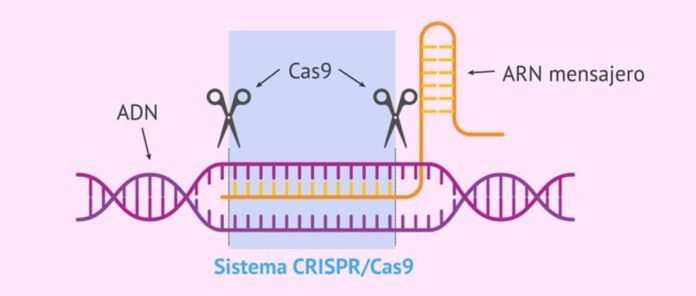
«Системи CRISPR-Cas» у бактеріях і вірусах ідентифікують і знищують вторгнення вірусних послідовностей. Це бактеріальна та архейна імунна система для захисту від вірусних інфекцій. У 2012 році система CRISPR-Cas була визнана геном інструмент редагування. З тих пір було розроблено широкий спектр систем CRISPR-Cas, які знайшли застосування в таких сферах, як генна терапія, діагностика, дослідження та поліпшення врожаю. Однак доступні на даний момент системи CRISPR-Cas мають обмежене клінічне використання через часті випадки нецільового редагування, несподівані мутації ДНК і спадкові проблеми. Нещодавно дослідники повідомили про нову систему CRISPR-Cas, яка може націлюватися на мРНК і знищувати її білки точніше пов’язані з різними генетичними захворюваннями без нецільового впливу та спадкових проблем. Це перша система CRISPR-Cas під назвою Craspase білок функція редагування. Це також перша система, яка може редагувати як РНК, так і білок. Оскільки Craspase долає багато обмежень існуючих систем CRISPR-Cas, він має потенціал для революції в генній терапії, діагностиці та моніторингу, біомедичних дослідженнях і покращенні врожаю.
«Система CRISPR-Cas» — це природна імунна система бактерій і архей проти вірусних інфекцій, яка ідентифікує, зв’язує та деградує послідовності у вірусному гені для захисту. Він складається з двох частин – бактеріальної РНК, транскрибованої з вірусного гена, включеного в бактеріальний геном після першого зараження (називається CRISPR, це ідентифікує цільові послідовності вторгнення вірусних генів), і пов’язаного руйнівника білок називається «CRISPR, пов’язаний білок (Cas)», який зв’язує та руйнує ідентифіковані послідовності у вірусному гені для захисту бактерій від вірусів.
ЧИСТКИЙ розшифровується як «згруповані регулярні короткі паліндромні повтори». Це транскрибована бактеріальна РНК, що характеризується паліндромними повторами.
Паліндромні повтори (CRISPR) були вперше виявлені в послідовностях E. палички у 1987 році. У 1995 році Франсіско Мохіка спостерігав подібні структури в архей, і саме він вперше подумав про них як про частину імунної системи бактерій і архей. У 2008 році було вперше експериментально продемонстровано, що мішенню імунної системи бактерій і архей є чужорідна ДНК, а не мРНК. Механізм ідентифікації та деградації вірусних послідовностей припустив, що такі системи можна використовувати як інструмент для редагування геному. З моменту свого визнання інструментом редагування геному в 2012 році система CRISPR–Cas пройшла дуже довгий шлях як міцно встановлений стандарт редагування генів система і знайшла широкий спектр застосувань у біомедицині, сільському господарстві, фармацевтичній промисловості, включаючи клінічну генну терапію1,2.
Широкий асортимент CRISPR- Системи CAS вже ідентифіковані та наразі доступні для моніторингу та редагування послідовностей ДНК/РНК для досліджень, скринінгу ліків, діагностики та лікування. Сучасні системи CRISPR/Cas поділяються на 2 класи (клас 1 і 2) і шість типів (тип I-XI). Системи класу 1 мають декілька Cas білки яким необхідно сформувати функціональний комплекс для зв’язування та дії на свої мішені. З іншого боку, системи класу 2 мають лише один великий Cas білок для зв’язування та деградації цільових послідовностей, що полегшує використання систем класу 2. Зазвичай використовуваними системами класу 2 є Cas 9 типу II, Cas13 типу VI та Cas12 типу V. Ці системи можуть мати небажані побічні ефекти, наприклад, нецільовий вплив і цитотоксичність3,5.
Генна терапія засновані на поточних системах CRISPR-Cas мають обмежене клінічне використання через часті випадки нецільового редагування, несподівані мутації ДНК, включаючи великі делеції фрагментів ДНК і великі структурні варіанти ДНК як у цільових, так і поза цільових ділянках, що призводить до загибелі клітин та інші спадкові проблеми.
Краспаза (або каспаза, керована CRISPR)
Дослідники нещодавно повідомили про нову систему CRISPER-Cas, яка є системою Cas2-7 класу 11 типу III-E, пов’язаною з каспазоподібною системою. білок тому названо Краспаза або каспаза, керована CRISPR 5 (Каспази - це цистеїнові протеази, які відіграють ключову роль в апоптозі в руйнуванні клітинних структур). Він має потенційне застосування в таких сферах, як генна терапія та діагностика. Краспаза керується РНК і націлена на РНК і не втручається в послідовності ДНК. Він може націлюватися і руйнувати мРНК і білки більш точно пов’язані з різними генетичними захворюваннями без нецільового впливу. Таким чином, елімінація генів, пов'язаних із захворюваннями, можлива шляхом розщеплення на рівні мРНК або білка. Крім того, при з’єднанні зі специфічним ферментом краспазу також можна використовувати для зміни функцій білків. Коли функції РНКази та протеази припиняються, Краспаза дезактивується (dКраспаза). Він не має функції розрізання, але зв’язується з РНК і білковими послідовностями. Тому dCraspase можна використовувати в діагностиці та візуалізації для моніторингу та діагностики захворювань або вірусів.
Craspase — перша система CRISPR-Cas, яка демонструє функцію редагування білка. Це також перша система, яка може редагувати як РНК, так і білок. Його редагування генів функція забезпечує мінімальний нецільовий ефект і відсутність успадкованих проблем. Отже, краспаза, ймовірно, безпечніша в клінічному застосуванні та терапії, ніж інші доступні на даний момент системи CRISPR-Cas 4,5.
Оскільки Craspase долає багато обмежень існуючих систем CRISPR-Cas, він має потенціал для революції в генній терапії, діагностиці та моніторингу, біомедичних дослідженнях і покращенні врожаю. Потрібні додаткові дослідження для розробки надійної системи доставки для точного націлювання на гени, що викликають захворювання, у клітинах, перш ніж підтвердити безпеку та ефективність у клінічних випробуваннях.
***
Список використаної літератури:
- Гостимська, І. CRISPR–Cas9: історія його відкриття та етичні міркування його використання в редагуванні геному. Біохімія Москва 87, 777–788 (2022). https://doi.org/10.1134/S0006297922080090
- Чао Лі та ін 2022. Обчислювальні інструменти та ресурси для редагування геному CRISPR/Cas. Геноміка, протеоміка та біоінформатика. Доступно онлайн 24 березня 2022 р. DOI: https://doi.org/10.1016/j.gpb.2022.02.006
- van Beljouw, SPB, Sanders, J., Rodríguez-Molina, A. та ін. РНК-націлені системи CRISPR–Cas. Nat Rev Microbiol 21, 21–34 (2023). https://doi.org/10.1038/s41579-022-00793-y
- Чуньї Ху та ін 2022. Краспаза — це РНК-керована CRISPR РНК-активована протеаза. Наука. 25 серпня 2022 р. Том 377, випуск 6612. С. 1278-1285. DOI: https://doi.org/10.1126/science.add5064
- Huo, G., Shepherd, J. & Pan, X. Craspase: новий редактор подвійних генів CRISPR/Cas. Функціональна та інтегративна геноміка 23, 98 (2023). Опубліковано: 23 березня 2023 р. DOI: https://doi.org/10.1007/s10142-023-01024-0
***